成都新华医院伦理委员会章程
发布时间:2022-09-01 来自:本站
发布时间:2022-06-14 本文来源: 新华医院
伦理审查申请指南
一、 研究范围:
药物临床试验、医疗器械临床试验
二、 伦理审查申请/报告类别:
1、初始审查申请:
符合上述范围的研究项目,应在研究开始前提前提交伦理审查申请。
2、跟踪审查:
1) 修正案审查申请:研究过程中若变更了主要研究者,或对临床研究方案、知情同意书、招募材料等进行了修改,应向伦理委员会提交修正案审查申请,经批准后执行。如果为了避免对受试者的即刻危险,研究者可以在伦理委员会批准前修改研究方案,但事后必须提出审查申请。
2) 研究进展报告:按照伦理审查批件/意见规定的年度/定期跟踪审查频率,在截止日期前1个月提交研究进展报告;若我院为临床研究的中心单位,申办者应向伦理委员会提交各个中心的研究进展汇总报告;如果伦理审查批件有效期到期,需要申请延长批件有效期,应通过“研究进展报告”申请。
3) 严重不良事件报告:严重不良事件是指临床研究过程发生需住院治疗、延长住院时间、伤残、影响工作能力、危及生命或死亡、导致先天畸形等事件。发生严重不良事件后应在获知24小时内向伦理委员会报告。
4) 违背方案报告:研究纳入了不符合纳入标准或符合排除标准的受试者;符合中止试验规定而未让受试者退出研究;给予错误治疗或剂量;给予方案禁止的合并用药等没有遵从方案开展研究的情况;或可能对受试者的权益/健康以及研究的科学性造成显著影响等违背GCP原则的情况。或研究者不配合监查/稽查,或对违规事件不予以纠正。凡是发生上述研究者违背GCP原则并可能对受试者的权益/健康以及研究的科学性造成显著影响的情况,监查员应提交违背方案报告等。
5) 暂停/终止研究报告:研究者/申办者暂停或提前终止已经获批的临床研究,应该及时向伦理委员会提交暂停/终止研究报告。
6) 研究结题报告:临床研究完成之后,应及时向伦理委员会提交研究结题报告。
3、复审:
按照伦理审查意见“作必要的修正后重审”,对方案进行修改后,应以“复审申请”的方式再次送审。
三、 伦理审查的流程:
1、提交送审文件
①送审责任人:研究项目的送审责任人一般为主要研究者。
②填写申请/报告的表格:根据伦理审查申请的报告类别,填写相应的“申请”。
③准备送审文件:根据送审文件清单要求,准备送审文件。
④提交:需提交1套加盖鲜章的送审文件,通过形式审查后准备13份复印件,送至伦理委员会办公室。
2、领取通知
①补充/修改送审材料通知:伦理委员会办公室受理后,如果认为送审文件不完整,文件要素有缺陷,发送补充/修改送审材料通知,告知缺项文件、缺陷的要素,及最近审查会议前的送审截止日期。
②受理通知:送审文件的完整性和要素通过形式审查,秘书发送受理通知,并告知预定审查日期。
3、接受审查的准备
①会议时间、地点办公室秘书提前电话通知。
②准备会议报告:报告人提前将上会PPT发送秘书,并提前10分钟到达会场。
四、 伦理审查的时间:
(一)伦理委员会每月例行召开审查会议1次,可根据需要调整或增加审查会议次数,可加急审查。
(二)伦理审查流程加速
(1)前置审批:
1、在未获得“国家药品监督管理局药物临床试验批件”的前提下,甚至于国家药审中心“默示许可公示”前,我中心伦理委员会可实施伦理前置审批。
2、前置伦理审批提交材料:《国家药品监督管理局行政许可文书受理通知书》;开展注册临床试验前与CDE沟通交流会议纪要或沟通函;其他。
(2)自行审批:
在组长单位伦理结果未出来或组长单位还未进行伦理审批的前提下,我中心伦理委员会可实施自行伦理审查。
(3)接受组长单位伦理:
我中心参与的多中心临床试验,我院伦理委员会接受组长单位伦理审查结果。
(4)我院牵头项目随到随审:
大力支持我院牵头项目,对我院牵头项目,伦理委员会实行随到随审制度:机构接到立项申请3个工作日内,伦理进行项目会议审查。
五、 审查决定的传达
1、会议审查:决定于会后3个工作日内形成书面审查意见/批件,报主任委员审签并传达。
2、紧急会议审查:决定于审查决定后及时传达,最长不超过2个工作日。
3、申请人在伦理委员会受理送审材料后一个半月内没有收到伦理委员会的审查意见,视为伦理审查意见为“同意”或者“不需要采取进一步的措施”。
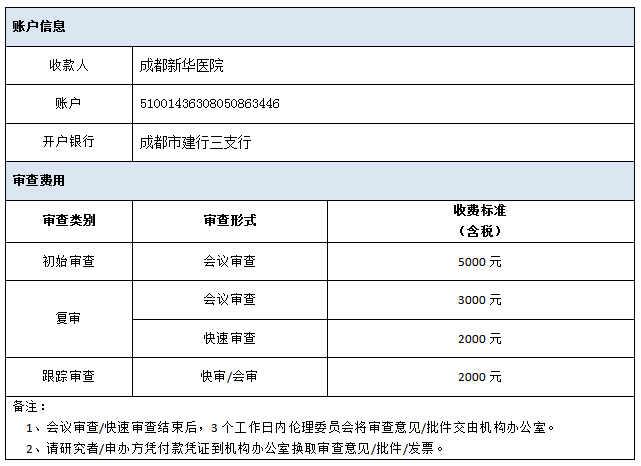
六、 伦理审查费用
各研究者/申办方,请在资料受理后至项目审查前尽快完成审查相关费用的支付,支付信息如下: